Après pas mal de recherches sur internet, on trouve peu de documents complets sur l’anodisation du titane, cette technique permet de colorer des objets en titane simplement avec des couleurs variées. Nous allons donc essayer de présenter ici de façon détaillée et compréhensible les expériences à réaliser pour anodiser le titane et les réactions chimiques lors de son anodisation.

Partie 1 : Anodisation du titane avec des produits chimiques « sans danger »
Expérience amusante, on peut en effet colorer son titane simplement avec des produits de tous les jours. Un schéma de l’expérience est présenté en partie 3.
Matériel :
– récipient en verre (type petit saladier)
– cuillère ou autre objet en Inox
– l’objet en titane
– du Coca-Cola ©
– du fil électrique (pour faire 2 câbles, du fil très fin suffit)
– des petites pinces crocos (pas indispensable mais vous faciliteront grandement la tâche)
– une pile 9V (celle rectangulaire)
Dans l’idéal votre pièce en Inox doit avoir une surface largement supérieure à celle de la pièce en titane. Pour le matériel que vous n’auriez pas voir la dernière partie « Annexe ».
Expérience :
Remplir le saladier de Coca, accrocher l’un des fils électriques à l’objet en Inox et l’autre fil à l’objet en titane. L’objet en Inox et celui en titane doivent être immergés dans le Coca (laisser dépasser la partie reliée au fil ou à la pince croco). Puis relier le fil électrique de l’objet Inox au pôle (-) de la pile et l’autre au pole (+), la réaction débute alors. Compter environ 15 secondes puis débrancher. La pièce s’est alors colorée en jaune foncé !
Suivant les conditions et la pièce à traiter, l’expérience est souvent déjà spectaculaire mais la couleur peut paraître peu homogène ou terne. Pour ceux qui le peuvent, vous trouverez ci-dessous l’expérience plus « pro » mais qui se réalise également avec des produits vendus aux particuliers.
Vous pouvez ajouter des piles en série pour obtenir d’autres couleurs.
Partie 2 : Anodisation du titane avec de l’acide sulfurique
Mise en garde : contrairement à l’expérience précédente qui présentait peu de risque, celle-ci doit être réalisée avec blouse, lunettes de sécurité et gants.
Matériel :
– récipient en verre (bécher, saladier, …)
– surface métallique ne pouvant pas être attaqué par l’acide (Cuillère Inox, Platine, Alu, …)
– objet en titane ou tige de titane
– acide sulfurique 37%
– câbles électriques (2 ou + si l’on veut surveiller la tension ou ajouter des piles)
– pinces crocos
– piles (les 9V en série permettent de changer assez nettement la couleur)
– facultatif : un voltmètre
Dans l’idéal votre pièce en Inox doit avoir une surface largement supérieure à celle de la pièce en titane. Pour le matériel que vous n’auriez pas voir la dernière partie « Annexe ».
Expérience :
Enfiler blouse, lunettes, gants, remplir le récipient en verre à 1/3 de sa contenance avec de l’eau, puis ajouter doucement la même quantité d’acide sulfurique (il reste 1/3 du récipient vide pour éviter les risques de débordement ou de déversement). Relier l’objet en titane et l’objet Inox chacun à un fil électrique différent. La surface métallique Inox et l’objet en titane doivent ensuite être immergés dans l’acide (laisser dépasser les parties reliées par les pinces crocos). La plaque ou cuillère en acier inoxydable doit être reliée au pôle (-) de la ou des pile(s), la pièce en titane doit être reliée au pôle (+), la réaction commence alors. Si vous le souhaitez, vous pouvez brancher un voltmètre (en dérivation !). Dans un premier temps, réaliser l’expérience avec une pile 9V et un temps de 15 secondes. Ensuite débrancher un des câbles et sortir la pièce : celle-ci est colorée (en jaune foncé normalement) !
Par la suite, vous pouvez augmenter ou diminuer le nombre de piles et surveiller la tension avec le voltmètre, les couleurs obtenues vont dépendre du voltage !
Partie 3 : Schéma de l’expérience
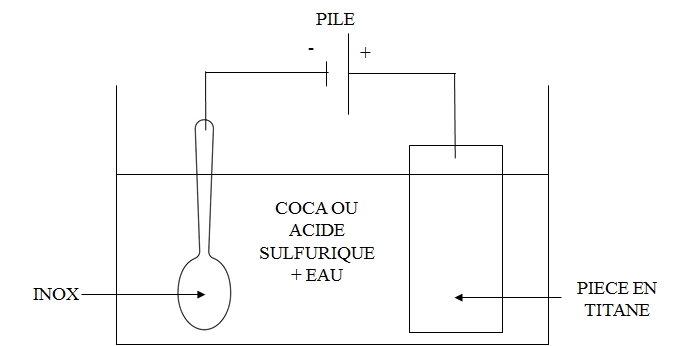
Partie 4 : Réactions chimiques lors de l’anodisation du titane
La réaction globale est une réaction d’électrolyse en milieu acide qui va conduire à la création de dioxyde de titane à la surface de notre pièce. On parle d’anodisation puisque l’objet en titane relié au pôle (+) sera l’anode (où aura lieu une oxydation) et la cuillère ou l’autre objet en Inox sera la cathode (où aura lieu la réduction). Dans un premier temps, on note que l’acide sulfurique se dissocie dans l’eau (acide fort) en 2H+ + SO42-. Dans le cas du Coca, les ions H+ proviennent en grande partie de l’acide phosphorique présent dans celui-ci. Puis les réactions suivantes se produisent :
A la cathode : H+ + e– –> ½ H2 (réduction), création de dihydrogène gazeux, c’est pourquoi on peut observer de petites bulles à la surface de la cathode.
A l’anode: Ti –> Ti4+ + 4e– (oxydation)
D’où la réaction globale pour l’électrolyse : Ti + 4H+ –> 2H2 + Ti4+
Puis a lieu la formation du dioxyde de titane (les ions titanium formés lors de l’oxydation réagissent avec l’eau présente dans notre solution) : Ti4+ + 2H2O –> TiO2 + 4H+
C’est cette couche d’oxyde de titane qui va conférer différentes couleurs à l’objet. Cette couche est particulièrement résistante ce qui permet une bonne coloration.
Partie 5 : pourquoi des couleurs différentes suivant les tensions ? Couleurs interférentielles et couleurs obtenues lors de l’anodisation en fonction de la tension
Le principe des différentes couleurs vient du fait que le dioxyde de titane produit des couleurs interférentielles, c’est à dire que la couleur dépend de l’épaisseur de la couche d’oxyde. C’est l’indice de réfraction élevé du dioxyde de titane (entre 2,5 et 2,8 pour des longueurs d’ondes correspondant à la lumière visible) qui permet ce phénomène.
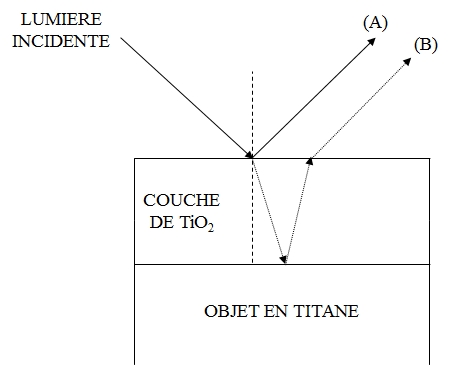
Une partie de la lumière est complètement réfléchie par la surface de la couche de dioxyde de titane. Mais une autre partie est transmise avec au passage réfraction en entrée de la couche de TiO2 puis réflexion lors de l’arrivée sur le titane lui-même puis à nouveau réfraction en sortie de la couche de TiO2. Les rayons (A) et (B) vont alors « interférer » et créer un effet « irisé » et des couleurs interférentielles.
Quelle couleur pour quelle tension ?
Le fait de faire varier la tension permet de faire varier l’épaisseur de dioxyde de titane et donc la couleur. On a grossièrement les couleurs suivantes :
– 10V –> jaune
– 20V –> bleu
– 40V –> bleu ciel
– 60V –> jaune – orange
– 75V –> violet
– 90V –> bleu-vert
Pour un spectre complet des couleurs, voir ce site.
Partie 6 : vitesse, variantes et autres possibilités
On notera qu’avec d’autres produits à disposition, l’anodisation du titane peut se faire par exemple avec de l’acide phosphorique ou d’autres solutions permettant d’obtenir une quantité de H+ suffisante. De plus, un temps de 15 seconde est indiqué ci-dessus mais la coloration se fait quasi-instantanément.
De plus, lors de l’anodisation, l’application de « caches » c’est à dire vernis spécifique ou scotch adéquat permet l’obtention de différents effets avec par exemple le reste de l’objet coloré et des zones qui ne le sont pas.
Annexe : le matériel
La plupart des éléments nécessaires à l’anodisation du titane se trouvent assez facilement. Toutefois, il faut savoir ou chercher :
– fils et pinces croco : vendus dans des « kits » avec pince à dénuder ou sur www.jeulin.fr (fils utilisés au lycée et dans mon montage, vente aux enseignants et établissement d’enseignement).
– acide sulfurique : magasin de bricolage ou automobile (acide pour batteries) type Castorama ou Feu Vert.
– le titane : c’est peut-être là le plus compliqué si vous n’avez pas d’objet en particulier à colorer ou à tester. Si vous n’en avez plus besoin, vous pouvez utiliser une ancienne monture de lunettes en titane (enlevez d’abord la couche colorée). Si vous voulez répétez l’expérience un grand nombre de fois achetez une tige ou un fil titane par exemple sur www.titane-services.eu (15€ de commande mini…). Si vous n’avez que deux ou trois expériences à réaliser pour satisfaire votre curiosité, celles de vos proches ou vous amuser, n’hésitez pas à nous contacter à blog@partiprof.fr. Nous pourrons vous faire parvenir 2 ou 3 morceaux de titane contre 2 timbres.
Voilà, vous êtes maintenant prêt pour colorer votre titane avec l’anodisation et détailler les phénomènes chimiques et physiques qui entrent en jeu !
Traitement post-anodisation
Suite à plusieurs questions par mail et en commentaires je me suis un peu plus renseigné sur les traitements qui existent pour pérenniser l’anodisation. Il semble qu’on puisse après celle-ci appliquer un vernis à base de molybdène ou de Teflon ® qui vont améliorer les propriétés de frottements (car à la base le revêtement est fin et supporte peu les manipulations). Si vous avez plus d’informations n’hésitez pas à partager !



J’ai envie d’essayer cette expérience rien que pour voir le résultat. Ce n’est pas dangereux mais est-ce qu’un enfant peut faire cette expérience? J’aime bien faire découvrir de nouvelles choses aux enfants. J’adore voir leur tête pleine d’étonnement.
Bonjour,
je pense que la première expérience avec le Coca ne présente pas spécialement de risque. Prévoyez tout de même de l’accompagner notamment pour les piles pour éviter les coups de jus…
Bonjour,
J’ai fait quelques réalisation en anodisation de titane avec de très bons résultats sur certaines couleurs en haut voltage. J’ai néanmoins quelques soucis de rendu de couleurs avec le marron, violet et bleu principalement. Mon problème est que la couleur qui semble pourtant uniforme dans le liquide se change lors du séchage et surtout réagis aux traces laissé par les doigts.
Je vous joins quelques photos:
Avant manipulation:

Après manipulation:

Les essais concluants:


Auriez vous un avis ou un conseil pour éviter ce genre de transformation de la couleur par la manipulation?
Merci d’avance pour votre aide.
Bonjour,
merci pour votre message. Pourriez-vous m’indiquer le protocole suivi ? (bain, générateur, temps dans le bain, temps de séchage, voltmètre ?, …)
Au passage les pièces réussies sont vraiment très belles. Afin de pouvoir vous répondre sur les couleurs obtenues à des voltages plus faibles, j’attends votre protocole. Quelques éléments de réponses tout de même : le pH et la température peuvent avoir une influence sur la structure de la couche de TiO2 obtenue notamment à bas voltages (suivant la composition de l’électrolyte). Mais ceci dépend beaucoup de la composition de l’électrolyte utilisé. Les dépôts étant généralement très fins, leurs adhérences ne peuvent généralement pas être mesurées car épaisseur trop faible, et ainsi la manipulation « arrache » la couche d’oxyde.
Bonjour et merci pour votre réponse.
Pour la préparation du titane afin de retirer la couche d’oxyde, j’utilise ce merveilleux produit qu’est le Multi Etch, après dégraissage à l’acétone. ce qui m’a permit de monter à des voltages plus conséquent car avant je ne pouvais pas dépasser le seuil des 50V sans cramer mon titane.
L’alimentation utilisée est une 0-120V / 1A.
Le bain est un bain d’eau distillée avec du TSP (sorte de lessive), je dois encore tester l’acide sulfurique dilué.
Je passe donc les tubes aux Multi Etch, puis rincés à l’eau distillée, et directement plongés dans le bain d’anodisation.
Mon anode est une barre de titane, que je pose directement au contact des pièces (à l’intérieur afin d’éviter de marquer le métal si il y a une étincelle)
Je commence toujours par le 10/12V puis je monte progressivement jusqu’au voltage visé. Je laisse l’anode posée jusqu’à ce que l’alim m’indique une valeur proche du 0 ampère.
Je vais tester de réchauffer l’electrolyte selon vos conseils.
Dans tous les cas, j’utilise toujours de l’eau distillée, et ce à toutes les étapes.
Merci pour vos conseils !
Re-bonjour,
merci pour le protocole. Pour le bain effectivement si vous pouviez avoir plus « la main » sur la composition ça pourrait être mieux, car pour le TSP avez-vous le détail de la concentration en Na3PO4 (c’est bien de ça qu’est composé votre bain ?) et autres ?
La préparation me semble adéquate ainsi que l’arrêt du traitement (à 0A). Pourriez-vous me préciser les voltages exacts à partir desquels vous n’avez plus de problèmes d’adhérence ?
Chauffer peut être une première solution, tenez moi au courant. Je pense qu’avoir la composition exacte du bain et contrôler le pH également.
Cordialement,
Jérémy.
Bonjour,
J’ai le même problème que présenté par « ANONYME » (uniquement sur les faibles voltages 5-25V au dela le problème disparait.
J’utilise également du TSP comme bain électrolyte.. peut-être que le problème vient de la, mais aujourd’hui, ce bain est celui qui m’ donné le meilleur résultat.
Avez vous entendu parlé d’une solution pour résoudre se probleme?
Existe il un vernis qui pourrait protéger l’anodisation sensible au traces de doigts sans en modifier la couleur?
Merci
Bonjour
Je fabrique des petits bijoux en titane ça me coûte très cher de les anodisés
Quel coup de génie le coca. Bravo. Le titane reste t’il toujours anti allergique ?????
Mon fil de titane est toujours mat ! Avez vous une astuce pour le rendre brillant à par de la toile emerie???
J’attends vos réponses avec beaucoup d’impatience
Merci mille fois
Cordialement
Bonjour,
merci pour votre message. Concernant les allergies la couche d’oxyde de titane est d’une épaisseur très faible, je ne pense donc pas qu’il y ait d’effet néfaste sur les propriétés du titane. Il faudrait se renseigner plus en détails sur les propriétés du TiO2. On peut lire sur Wikipédia « Le TiO2 ne semble pas allergène » ce qui ne nous avance pas beaucoup pour des couches plus épaisses…
Concernant la brillance, non je n’ai pas de produit particulier connu… Peut être la préparation de la pièce en amont, ou un bain de brillanteur. Bon courage pour vos futures anodisations !
Cordialement,
Jérémy,
Bonjour,
Dans votre palette de couleur, vous ne parler pas de la teinte noire.
Serait-il possible de connaitre le procédé pour obtenir cette teinte ?
D’avance merci
Cordialement
Bonjour,
Merci pour votre message. Effectivement le noir n’apparaît pas dans l’échelle de teinte. Je n’ai jamais observé de titane anodisé noir. En revanche la teinte noire peut être obtenu « simplement » par la technique de déposition en phase vapeur PVD.
Bonjour,
Je cherche également à obtenir une teinte noir pour un bijoux. La technique de déposition en phase vapeur est-elle accessible à un amateur ? Il semble, d’après ce que j’ai pu lire, que cela nécessite des moyens assez conséquents : gaz rare, pour travailler sous vide, …
Merci
Bonjour Jérémy,
Enseignant en technologie à la retraite,
je fais de l’anodisation du titane sur feuille mince ( 0,5 mm). bain acide sulfurique à 10 % tensions de 25 à 65 volts. pour passer à des épaisseurs de 1 a 3 mm quelle densité de courant faut-il respecter pour obtenir un bonne anodisation ? .
je vais acheter un alimentation variable et ne sait pas quelle intensité choisir entre 3 ou 5 ampères.
merci pour votre aide
Bonjour,
merci pour votre message. Je n’ai pas d’infos complète sur l’intensité mais pour les traitements de surface la densité de courant est fonction de la surface de la pièce donc cela dépend déjà de la taille de la pièce à anodiser. Dans tous les cas dans un premier temps il vaut mieux partir sur 3A puis sur 5A si tout se passe correctement afin d’avoir un dépôt plus rapide.
Cordialement,
Jérémy.
Bonjour,
J’ai fait le test avec des piles 9V, sur des anneaux de canne à pêche en titane.
Par contre, alors que les pièces à traiter sont relativement fines et petites, cela met longtemps pour se colorer (plusieurs minutes !!).
Comment puis-je accélérer le processus ?
j’ai un bain d’acide sulfurique, et une plaque d’inox d’environ 30X50 mm.
Merci pour vos conseils,
JC
Bonjour,
merci pour votre message. Votre constatation est assez étonnante car l’anodisation se fait « plutôt » rapidement normalement. J’ai beaucoup de questions : Avec combien de piles 9V travaillez-vous ? Et vous parlez de bain d’acide sulfurique : quelle est sa concentration ? Les pièces sont-elles entièrement en titane ? Et quelle est la taille d’une pièce ?
Peut-être qu’avec ses informations nous pourrons trouver un moyen de régler ce « problème ».
Jérémy.
Bonjour !
Tout d’abord merci pour ce tuto juste génial et complet !!!
J’aimerai apprendre cette technique pour un projet pro donc il me faut quelque chose de durable dans le temps !
J’aurai donc quelques questions 🙂
1- Faut-il nettoyer, traiter le métal avant dans une solution chimique aussi ?
2- Suite à l’anodisation, on nous parle d’un traitement de surface (fixation) dans une solution d’acide cathodique… Important pour fixer la couleur apparemment ! Cela vous parle-t-il ?
3- J’aimerai réaliser cette expérience mais avec de l’acier inoxydable type 316L, pour de la bijouterie, est ce possible ? Est ce que cela marche de la même manière ? sauf que l’on inverse les source de courant + et – ?
Merci beaucoup !!!!!!!
Bonjour Manon,
merci pour votre message ! Content que cela puisse vous aider. Je vais essayer de répondre à vos questions :
1/ Oui si c’est quelque chose de professionnel, c’est un élément capital du traitement de surface, la pièce doit être nettoyée et dégraissée.
La préparation de la pièce dépend beaucoup de l’usinage qui a été fait, de son procédé de fabrication. En effet elle sera plus ou moins « sale ».
L’opération peut-être par exemple un dégraissage (pas avec un solvant chloré pour ne pas fragiliser le titane) puis
dans certains cas opération de décapage mais ce n’est pas forcément nécessaire suivant le but recherché. On peut ensuite procéder à l’anodisation.
2/Pouvez-vous me donner les références vous indiquant cette fixation ? Peut-être avez-vous confondu avec l’anodisation de l’aluminium où là
une opération de colmatage est nécessaire.
3/ Non malheureusement ce n’est pas aussi simple, comme indiqué en fin d’article les couleurs obtenues sont dues à l’oxyde de titane qui produit des couleurs
interférentielles. Inverser les bornes ne produira pas de coloration.
En espérant que ceci vous apporte des réponses, n’hésitez pas si vous avez d’autres questions !
Jérémy
Bonjour Monsieur,
J’ai, hier, tenté de réaliser l’anodisation des tiges de titane que vous m’aviez fournies sans réel succès. J’ai suivi le protocole détaillé sur votre site : j’ai utilisé un bêcher avec de l’acide sulfurique et de l’eau, un générateur de tension continue (à la place des piles) et une électrode de platine. Cependant, je n’ai rien remarqué que ce soit la couleur sur la tige de titane ou le dégagement gazeux au niveau de mon électrode de platine car il n’y avait aucun courant qui circulait. Selon mes professeurs, cela serait du au fait que le titane, très réducteur, s’oxyde déjà très bien spontanément et possède donc déjà une couche de TiO2 trop importante pour qu’il s’oxyde davantage et donc empêchant l’existence d’un courant.
J’ai donc plusieurs questions à vous poser à ce sujet :
– Si le titane est déjà oxydé, pourquoi n’observe-t-on pas de couleurs sur sa surface ?
– Comment avez-vous réalisé votre expérience pour qu’elle fonctionne ? Mes profs m’ont conseillé pour la prochaine fois de frotter la tige en titane pour enlever la couche d’oxyde et de réaliser l’expérience juste après. Pensez vous que cela puisse fonctionner ?
Merci d’avance.
Bonjour,
merci pour le message. Étonnant que la réaction n’ait pas fonctionné, car j’ai pu la réaliser avec des conditions expérimentales très diverses, ainsi que d’autres internautes (en effet la réaction fonctionne même avec de l’eau seule).
Plusieurs points sont à vérifier :
– avez-vous bien placé la pièce en titane à l’anode (borne + du générateur) et l’électrode de platine au pôle – ?
– qu’affiche un ampèremètre branché (en série) dans le circuit ?
– avez-vous choisi une tension qui permette d’obtenir une couleur bien différente de la couleur initiale (voir le spectre sur le site) ?
– quelle est la taille de l’électrode en platine ? Comment l’avez-vous positionnée par rapport à la tige ?
– avez-vous essayé avec une électrode en inox ?
Par rapport aux remarques de vos enseignants la préparation de surface est effectivement importante dans le cas d’un traitement, disons « industriel », dans lequel il faut que la couche recherchée accroche et ait des propriétés particulières. Je crois que ce n’est pas ce que vous cherchez ? Pour la remarque concernant l’oxydation effectivement le titane est réducteur mais les oxydes « éventuellement » formés n’empêchent pas la réaction, même sans préparation de surface particulière.
Tenez-moi au courant de vos résultats. Cordialement,
Jérémy
Bonjour,
Concernant les points de l’expérience à vérifier, mon circuit était bien dans le bon sens et une mesure de courant avec un ampère mètre indiquait un courant nul. Au niveau de la tension, je n’ai pu monter que jusqu’à 30V car j’ai utilisé un générateur de tension continue qui ne pouvait pas monter plus. J’essaierai avec une électrode d’inox ou d’aluminium pour voir s’il y a du changement. Enfin je me suis rendu compte que cela pouvait également être du à la petite taille de mon électrode de platine (celles utilisées pour les mesures de potentiel ) qui était plus petite que la tige de titane.
Merci beaucoup pour votre aide.
Cordialement
merci pour vos infos par contre j’ai lu qu’il fallait protéger l’anodisation. Savez-vous ce qu’est ce lubrifiant au nom savant ?
merci encore
« Après le traitement d’anodisation, un traitement complémentaire sera souvent appliqué. Il pourra s’agir d’une peinture ou d’un lubrifiant sec tel que vernis à base de MoS2 ou de P.T.F.E. «
Bonjour, ce sont des lubrifiants qui permettent effectivement une protection après traitement. Celui à base de MoS2 : sulfure de molybdène, celui à base PTFE : Teflon (https://www.usinenouvelle.com/expo/vernis-sec-au-ptfe-teflub-p233343.html). Je ne connais pas en détail ces différentes protections mais le vernis à base de Teflon offre une bonne résistance, suivant les conditions auxquelles sera exposé l’objet par la suite.
Comme j’ai eu différents échanges par mail sur ce sujet susceptibles de vous intéresser, voici un échange de mail en commentaires :
Bonjour Monsieur,
J’ai, hier, tenté de réaliser l’anodisation des tiges de titane que vous m’aviez fournies sans réel succès. J’ai suivi le protocole détaillé sur votre site : j’ai utilisé un bêcher avec de l’acide sulfurique et de l’eau, un générateur de tension continue (à la place des piles) et une électrode de platine. Cependant, je n’ai rien remarqué que ce soit la couleur sur la tige de titane ou le dégagement gazeux au niveau de mon électrode de platine car il n’y avait aucun courant qui circulait. Selon mes professeurs, cela serait du au fait que le titane, très réducteur, s’oxyde déjà très bien spontanément et possède donc déjà une couche de TiO2 trop importante pour qu’il s’oxyde davantage et donc empêchant l’existence d’un courant.
J’ai donc plusieurs questions à vous poser à ce sujet :
– Si le titane est déjà oxydé, pourquoi n’observe-t-on pas de couleurs sur sa surface ?
– Comment avez-vous réalisé votre expérience pour qu’elle fonctionne ? Mes profs m’ont conseillé pour la prochaine fois de frotter la tige en titane pour enlever la couche d’oxyde et de réaliser l’expérience juste après. Pensez vous que cela puisse fonctionner ?
Merci d’avance.
Bonjour,
merci pour le message. Étonnant que la réaction n’ait pas fonctionné, car j’ai pu la réaliser avec des conditions expérimentales très diverses, ainsi que d’autres internautes (en effet la réaction fonctionne même avec de l’eau seule).
Plusieurs points sont à vérifier :
– avez-vous bien placé la pièce en titane à l’anode (borne + du générateur) et l’électrode de platine au pôle – ?
– qu’affiche un ampèremètre branché (en série) dans le circuit ?
– avez-vous choisi une tension qui permette d’obtenir une couleur bien différente de la couleur initiale (voir le spectre sur le site) ?
– quelle est la taille de l’électrode en platine ? Comment l’avez-vous positionnée par rapport à la tige ?
– avez-vous essayé avec une électrode en inox ?
Par rapport aux remarques de vos enseignants la préparation de surface est effectivement importante dans le cas d’un traitement, disons « industriel », dans lequel il faut que la couche recherchée accroche et ait des propriétés particulières. Je crois que ce n’est pas ce que vous cherchez ? Pour la remarque concernant l’oxydation effectivement le titane est réducteur mais les oxydes « éventuellement » formés n’empêchent pas la réaction, même sans préparation de surface particulière.
Dernier point : afin d’aider les autres, puis-je publier votre message de manière anonyme sur l’article du blog ?
Tenez-moi au courant de vos résultats. Cordialement,
Jérémy Tellier.
Bonjour Monsieur,
Veuillez m’excusez de ne revenir vers vous que maintenant, je devais bien avancer ma partie théorique et n’ai donc pas eu beaucoup de temps pour mes expériences. J’ai finalement réussi à effectuer l’anodisation du titane sur les tiges que vous m’aviez envoyées mais également sur des plaques en titane que j’ai pu me procurer via le lycée comme vous pouvez le voir sur ces photos. Cela a fonctionné grâce au changement d’électrode que vous m’aviez conseillé: je me suis servi d’une plaque d’aluminium.
J’ai essayé de contacter des entreprises mettant en oeuvre ce procédé afin d’en savoir un peu plus sur les techniques industrielles mais je n’ai pas eu de réponses pour cause de confidentialité. J’aurais donc aimé savoir si vous connaîtriez vous-même les techniques utilisées en industrie ainsi que des domaines d’applications autre que le domaine médical.
Par ailleurs, j’aimerais étudier les limites de cette couche de TiO2 en plongeant mes pièces de titane dans certains milieux susceptibles de la faire disparaître. Connaissez-vous de tels milieux ?
http://www.partiprof.fr/img/pieces-anodisation-titane.jpg
http://www.partiprof.fr/img/pieces-anodisation-titane-bis.jpg
Bonjour,
merci pour votre retour et ses photos intéressantes. Vous avez un bon rendu. Pour votre question ayant travaillé en entreprise auparavant je suis également tenu par certaines réserves car les accords de confidentialité sont encore valables. Toutefois pour votre question la technique industrielle (celle que je connais en tout cas) repose sur le même principe de base, mais avec un bain plus optimisé (pH, température, …), ainsi que les paramètres (intensité, taille des électrodes, …). Les domaines d’applications sont effectivement en partie le médical mais aussi décoratif : les couteaux « Balisong » ou les « flashlights » par exemple sont souvent colorés par anodisation (http://bit.ly/2mTwq0y). J’ai également plusieurs « petits » bijoutiers qui me posent des questions sur la technique car elle est peu onéreuse pour colorer des boucles d’oreille par exemple.
Pour la couche de dioxyde de titane celle-ci est très résistante aux attaques chimiques c’est pourquoi on s’en sert parfois comme protection du titane. Seul l’acide fluorhydrique ou des dérivés pourrait l’attaquer, mais il est difficile de s’en procurer et c’est une solution très toxique et très corrosive, qu’on ne vous laissera pas utiliser, je pense. Par contre la méthode physique parait plus raisonnable si l’épaisseur n’est pas trop grande, on peut « polir » la pièce avec une « Dremel » par exemple, le problème étant que le titane pourra aussi être un peu attaqué.
En espérant avoir tout de même pu répondre à certaines de vos questions je reste disponible pour d’autres questions. Bon travail pour la suite de votre TIPE,
cordialement,
Jérémy Tellier.
Bonsoir Monsieur,
Afin d’ajouter un résultat plus quantitatif à mon étude, j’ai mesuré le courant de corrosion de mes différentes pièces anodisées à l’aide d’un potentiostat afin de bien mettre en valeur le fait que les pièces avec une épaisseur de couche d’oxyde plus importante laissait passer un courant plus faible et était ainsi plus protégées. Cependant, lors d’un exercice d’entrainement de présentation de mon travail, un de mes professeurs paraissait dubitatif quant au seul rôle des couleurs interférentielles dans la coloration du titane. En effet, certaines photos prises sur un site de dispositifs médicaux montraient des objets tels que des vis colorées uniformément ce qui ne peut pas résulter uniquement de couleurs interférentielles, l’objet étant courbées (vis).
J’aurais donc aimé savoir si, d’une part, la coloration des pièces de titane que j’ai anodisées à l’aide de votre protocole est uniquement due aux couleurs interférentielles, auquel cas je pourrais avoir un ordre de grandeur de l’épaisseur d’oxyde à l’aide d’un processus optique et d’autre part si vous saviez d’où peut provenir la coloration de telles pièces industrielles si les couleurs interférentielles ne sont pas le seul phénomène à prendre en compte.
J’espère avoir été assez clair et vous remercie par avance.
Bonjour,
pour votre message concernant les pièces courbées, je pense que vous avez dû voir sur le blog les photos d’un internaute avec des pièces cylindriques, qui sont colorées uniformément. De même j’avais pu mettre au point un process pour des branches de lunettes. La courbure de la pièce n’empêche pas la formation d’oxyde à sa surface.
Pour l’épaisseur la prise de masse est envisageable avec un dispositif adéquat (il faut connaitre la masse d’oxyde déposée par pesée, la surface de la pièce et plus difficile estimer la masse volumique de l’oxyde). Sinon je ne suis pas expert dans ce domaine mais la réflectométrie me parait utilisable comme processus optique.
N’hésitez pas si ceci ne répond pas à vos questions je ne suis pas sûr d’avoir bien compris ce que voulait « dire » votre enseignant.
Cordialement,
Jérémy Tellier.
Bonsoir Monsieur,
En fait, mon professeur m’avait expliqué que ce qu’on appelle phénomène de couleurs interférentielles entraîne la présence de différentes couleurs en fonction de l’angle d’incidence de la lumière avec laquelle on éclaire l’objet. Ainsi, pour certains objets comme des vis, l’angle d’incidence de la lumière n’est pas le même sur toute la surface de l’objet et la couleur perçue ne devrait donc pas être uniforme ce qui n’est pas le cas. J’ai donc du mal à comprendre comment ces objets peuvent ils être colorés uniformément, le phénomène de couleurs interférentielles ne pouvant pas être le seul à prendre en compte.
Merci encore pour vos réponses.
Bonjour,
d’accord je n’avais pas bien compris la remarque. Effectivement les couleurs interférentielles dépendent de l’angle d’observation (voir les plumes de colibris par exemple). Toutefois (pour les pièces que j’ai déjà anodisées et celles vues en industrie) ceci n’est pas visible (à l’œil en tout cas).
Avez-vous essayé des anodisations avec des pièces courbées ou ayant des recoins ? Il pourrait ainsi être intéressant de varier l’angle d’incidence de la lumière et de « mesurer » la couleur avec un spectrocolorimètre, le problème étant que je ne suis pas certain qu’on puisse orienter la pièce comme on le souhaite dedans.
Il n’est pas rare que les traitements de surface soient combinés avec d’autres, toutefois sans traitement supplémentaire on obtient bien quelque chose « d’uniforme » à l’œil (voir commentaires des bijoutiers « amateurs » pour des pièces avec beaucoup d’aspérités). Je ne suis donc pas catégorique sur ce point mais je pense que la différence de couleur due à l’angle d’incidence n’est pas assez importante pour qu’on puisse l’observer à l’œil nu (des calculs avec les indices de réfraction sont peut-être possibles d’ailleurs ?).
Par ailleurs votre travail étant très intéressant et je pense pouvant aider pas mal de personnes sur ce sujet, est-il possible de publier nos échanges de questions de manière anonyme sur le blog ?
N’hésitez pas si vous avez d’autres questions et tenez moi au courant si des mesures de couleurs sont effectuées.
Cordialement,
Jérémy Tellier.
Bonjour Monsieur,
Merci beaucoup pour votre réponse très détaillée.
Il n’y a aucun problème pour que vous publiez nos échanges sur le site.
J’ai essayé de faire une étude optique à l’aide d’un spectrophotomètre à fibre optique en éclairant mes différentes plaques de titane mais je n’ai pas encore bien pu exploiter les courbes obtenues, je vous tiendrais au courant.
Cordialement
Bonjour,
J’ai réalisé l’expérience avec le bain d’acide sulfurique avec une pièce en titane grade 5 (105mm x 55mm x 13mm) et une alimentation 120v / 10A.
J’ai observé un ampérage très élevé (8A) pour 60V donc je ne pouvais pas augmenter les Volts car il y avait trop d’ampère, alors que sur les vidéos que j’ai pu regarder l’ampérage ne dépasse pas 1A.
Est ce que la surface à anodisé fait varié l’ampérage ?
j’ai également observé une réaction sur la pièce en inox qui était recouverte de petite bulle lors de la mise en tension dans le bain…
Faudrait t’il chauffer le bain ? Utiliser de l’eau distiller ?
Merci d’avance pour vos réponses.
Bonjour,
merci pour votre message. L’ampérage parait effectivement élevé, il varie toutefois avec la pièce oui. A quelle concentration d’acide sulfurique était votre bain ?
D’autre part si je ne me trompe pas le titane grade 5 est un titane allié ? Les bulles sont caractéristiques du dégagement probable de dihydrogène. Avez-vous essayé avec du titane plus « pur » ?
Bonne soirée !
Bonjour
je voudrais avoir la couleur noir sur le titane comment dois je m y prendre
En vous remerciant
Bonjour,
merci pour votre commentaire, il n’est en fait apparemment pas possible d’obtenir la teinte noire par anodisation du titane. Suivant les possibilités que vous avez et le but recherché la teinte noire peut être obtenue par la technique de déposition en phase vapeur (PVD).
Bonjour,
Merci pour ce tutoriel vraiment très intéressant.
J’aimerais également teinter du titane en noir pour un bijoux. La technique de déposition en phase vapeur est-elle accessible pour un amateur ? De ce que j’ai pu voir sur le net, cela semble nécessiter de « gros moyens » : gaz rare, travail sous vide, … Pensez-vous que c’est réalisable ?
J’aimerai également anodiser une même pièce en plusieurs couleurs. Est-il possible de procéder à plusieurs anodisations successives avec des tensions différentes ? Mon idée serait de commencer par une anodisation avec la tension la plus élevée pour une couleur A, puis polir certaines parties et re-anodiser avec une tension plus basse pour obtenir une couleur B. Cela ne va-t-il pas altérer les parties en couleur A ?
Merci
Jérôme
Bonjour Jérôme,
merci pour votre commentaire. Content que l’article ait pu vous aider.
La technique PVD n’est effectivement pas accessible « de chez soi », ni même dans un laboratoire simple. Il faut des équipements spécifiques et notamment des tensions importantes.
Pour la deuxième partie, n’est-il pas possible de seulement masquer les parties à ne pas colorer, puis changer ensuite l’emplacement du masquage ?
Bonne journée,
Jérémy.
Bonsoir,
Votre article est très bien mais j’aurais encore quelques question:
1) Une fois la pièce anodisée et sèche, se marque-t-elle facilement ? que ce soit par les doigts ou un léger choc ?
2) Quand vous dites « Cette couche est particulièrement résistante ce qui permet une bonne coloration. » est ce que cela signifie que c’est une résistance aux chocs ? ou uniquement à la corrosion ?
3) Est-t’il facile d’obtenir la couleur voulue (assez précisément en fonction des tensions) et de pouvoir la reproduire ultérieurement sur une autre pièce ?
4) Je connais différents procédés tels que le PVD et le DLC pour obtenir une coloration du titane en noir, mais en connaissez-vous d’autres ?
Merci beaucoup
Bonjour,
merci pour votre commentaire. J’essaie d’apporter quelques éléments de réponses à vos questions :
La résistance de la pièce dépend apparemment beaucoup du protocole suivi (bain, générateur, temps dans le bain, temps de séchage, …).
Quelques éléments de réponses tout de même : le pH et la température peuvent avoir une influence sur la structure de la couche de TiO2 obtenue notamment à bas voltages (suivant la composition de l’électrolyte). Les dépôts étant généralement très fins, leurs adhérences ne peuvent pas être mesurées car l’épaisseur est trop faible, et ainsi la manipulation « arrache » la couche d’oxyde.
Je parlais donc pour la résistance à la corrosion.
Il est assez facile d’obtenir la couleur voulue mais je n’ai pas fait d’essais de répétabilité, avec des mesures précises de la couleur. Je pense toutefois qu’il faut dans ce cas également bien veiller à la composition du bain utilisé.
Je n’ai pas d’autres idées en tête pour la teinte noire, hormis le PVD et le DLC oui.
Si toutefois d’autres ont des réponses complémentaires je suis preneur 🙂 !
Bonjour puis je réalisé une anodisation sans acide sulfurique et avec une couche de couleur sufisante et une belle couleur merci
Bonjour,
merci pour votre commentaire. Cela dépend déjà pas mal de la pièce de départ et de ce que vous souhaitez pour « une couleur suffisante » ?
Bonjour,
Merci pour le tutoriel et aussi pour les éléments de réponses apportés.
je connais parfaitement cette technique d’anodisation et le processus d’obtention de la couleur sur le titane pur.
le TiO2 produit la couleur et la couleur dépend de l’épaisseur de la couche. C’est l’indice de réfraction du TiO2 ( 2.5 et 2.8) qui permet ce phénomène d’interférence.
Mon but aujourd’hui est de pouvoir désanodisé, en gros éliminer la couche d’oxyde formée. Pour cela j’aimerais savoir si vous avez réalisé des essais du genre. si oui, avez vous une idée des paramètres qui pourraient avoir une influence considérable.
Cordialement
Bonjour,
très intéressant ce tuto, j’ajoute une petite précision, il est possible de modifier la couleur en passant la tension supérieure mais pas l’inverse. Pour désanodiser le titane, j’applique de l’acide en pâte qui sert à nettoyer les soudures, ça fonctionne très bien, j’ai pas essayer avec de la soude, à voir.
Bonjour, votre site est super intéressant!
Question : est-il possible de remplacer l’acide sulfurique par de l’acide chlorhydrique?