Le tartre est souvent un ennemi, que ce soit dans les bouilloires, dans les éviers ou dans les salles de bains, il suffit de voir toutes les publicités et produits existants pour « l’éliminer ». Mais quel est le mécanisme de formation du tartre ?
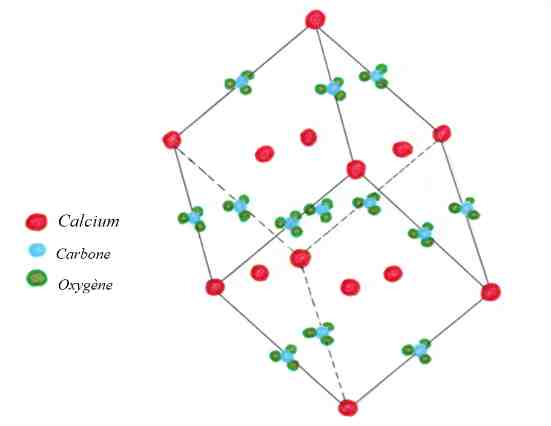
Tout d’abord il faut savoir que lorsque l’on parle de tartre on parle d’un composé essentiellement formé de carbonate de calcium CaCO3 (nous parlons ici uniquement du tartre dans l’eau) :
Le mécanisme de formation du tartre
D’un point de vue cristallochimique, le carbonate de calcium existe sous trois formes : la calcite, l’aragonite et la vatérite, ces deux dernières sont des variétés métastables de la calcite, c’est-à-dire qu’elles se transforment très lentement en calcite.
Nous allons détailler ici une des applications du carbonate de calcium : la formation du tartre et son mécanisme.
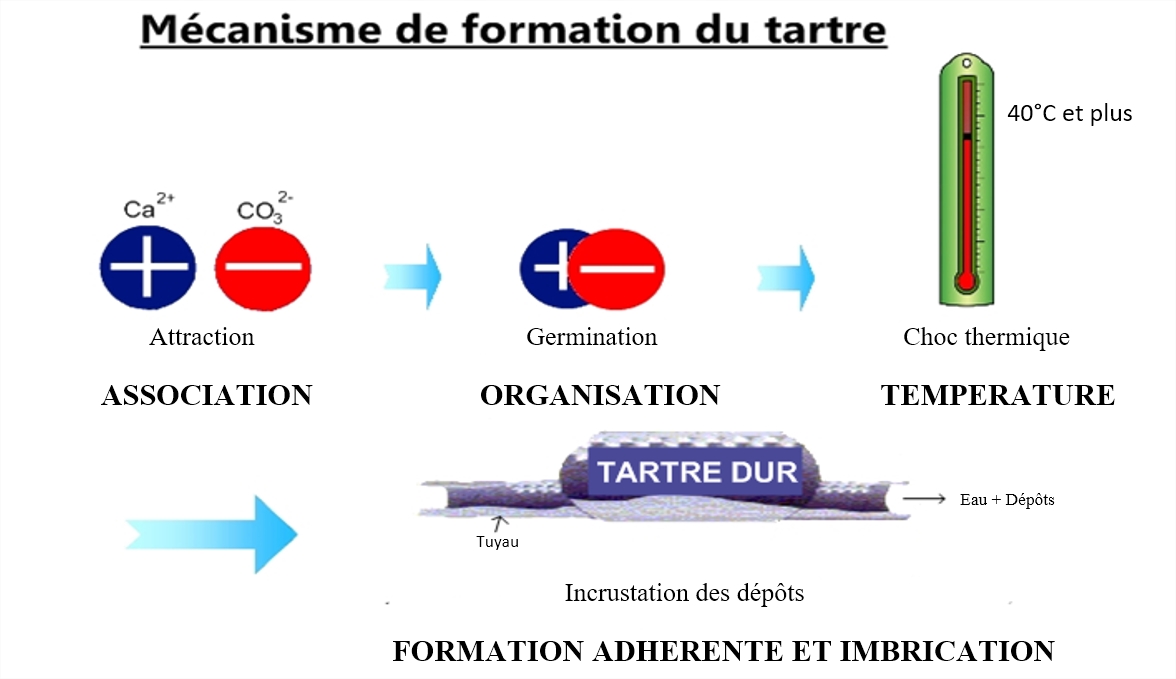
Le mécanisme de la formation du tartre fait intervenir trois étapes principales :
1. Les ions calcium Ca2+ et carbonate CO32- s’attirent de part leurs charges opposées.
Cette étape est appelée ASSOCIATION.
2. Ensuite il y a une germination homogène ( même probabilité de formation d’un « germe »
dans tout l’espace) puis une croissance des cristaux.
Cette étape est appelée ORGANISATION.
3. Avec l’élévation de température de l’eau (choc thermique) il se crée une précipitation organisée suivie d’une incrustation de forme adhérente.
Cette étape est appelée IMBRICATION.
Ce schéma résume le mécanisme de formation du tartre :
Bien évidemment le tartre / carbonate de calcium a aussi des applications plus « bénéfiques » : il peut servir dans la construction (ciment, chaux, …) et comme fondant dans la métallurgie.
Concernant l’élimination du tartre il existe nombreuses publications et recherches portant sur les différents traitements anti-tartre ( notamment traitement grâce au magnétisme).